有機化学において反応機構は、反応の本質を理解するために極めて重要ですが、しっかりとその意味について理解できている人は多くありません。
その理由の一つに反応機構の矢印があります。反応機構での矢印の意味をしっかりと理解している人は以外と少ないので、
当然矢印を使った反応機構の意味も理解できない人が多くなります。
今回は、そんな反応機構の矢印の種類、意味そして書き方を丁寧に説明していきます。
反応機構の矢印の種類とその意味
反応機構を書く時に注意しておくのは矢印です。
有機化学の教科書に書いてある反応機構にはしばしば曲がった矢印が登場します。
この矢印は、注意しておかなければ勘違いをしてしまいがちなので、最初に矢印の種類を理解しておきましょう。
矢印の種類:半矢印と両矢印
次の図をみてください。
これらはホモリシス開裂とヘテロリシス開裂という二つの分子の開裂の仕方を表しています。(画像出典:wikipedia)
ホモリシス開裂(Homolysis cleavage)
![]()
ヘテロリシス開裂(Heterolysis cleavage)
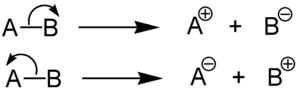
このとき、上のホモリシス開裂の赤い矢印をみてください。
よくみると、この矢印は先が半分しかない半矢印です。
半矢印が意味するのは、一つの電子の移動です。
つまり、上の図では電子対の2つの電子がそれぞれの原子に一つずつ移動したことを意味します。
次に、下のヘテロリシス開裂では、半矢印ではなく普通の矢印になっています。
この両矢印の場合には、電子対の移動を意味します。
つまり、電子対の2つの電子がどちらも同じ原子に移動することを意味します。
両矢印 ・・・ 電子対(2つの電子)の移動
矢印の出発点と終着点
矢印の出発点
次は反応機構における矢印の出発点についてみてみましょう。
先ほど確認したように先端が半分の半矢印では、電子一つの移動であるため、このときの矢印の出発点はその電子であると直感的にわかるでしょう。
それでは両矢印の場合はどうでしょうか?
両矢印では電子対(2つの電子)の移動を意味しているので、矢印の出発点はその電子対になります。
仮に、移動する電子が共有電子対で二つの原子の間で共有されている場合には、その矢印の出発点はその共有結合からになります。

↑矢印は共有結合からでている。(出典:wikipedia)
矢印の終点
矢印の出発点について説明したので、次は反応機構での矢印の終点について確認します。
矢印の終点は当然、その電子を保持する原子の方に向くわけですが、一部例外もあります。
その例外とはπ結合を作る時です。
π結合とは、二重結合や三重結合をつくるときに、もとあった単結合(σ結合)に加えて作られる結合です。
π結合を作る時には、もともと共有電子対が存在しているので反応機構をわかりやすくするためにもとあった結合に矢印の終点がきます。
・両矢印の出発点は非共有電子対か、共有結合(共有電子対)。
・矢印の終着点は原子か、もともとある結合(π結合を作る場合)。
矢印の注意点と矢印が作るもの
矢印の注意点:電子はある原子に保持され続ける。
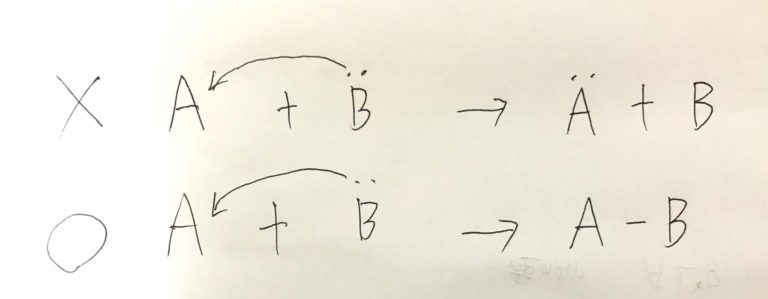
さきほど、両矢印が電子対の移動を表すことを確認しましたが、ここで注意してほしいのは、電子二つが完全に他の原子に飛ぶことはないということです。
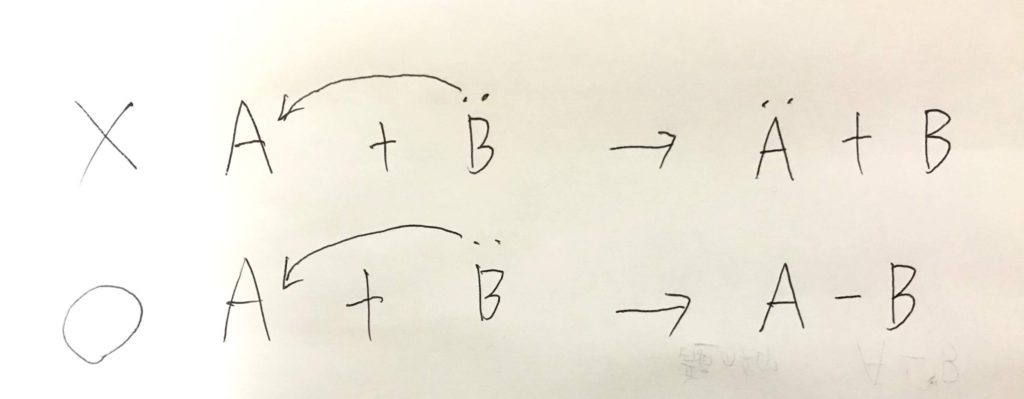
図でいうと、こういうことになります。Bの非共有電子対から出た矢印はAに入っていきますが、決してAに全て渡されるわけでなく、共有電子対(α結合)という形でBも保持しています。
このように、矢印の出発点と終着点で2つの電子は必ず一つの原子(この場合はB)が共通して保持し続ける性質があります。
共有結合から矢印が出発した時、どちらの原子がその電子を保持するか怪しくなりますが、その場合、曲がった矢印の内側にある原子が保持することになります。
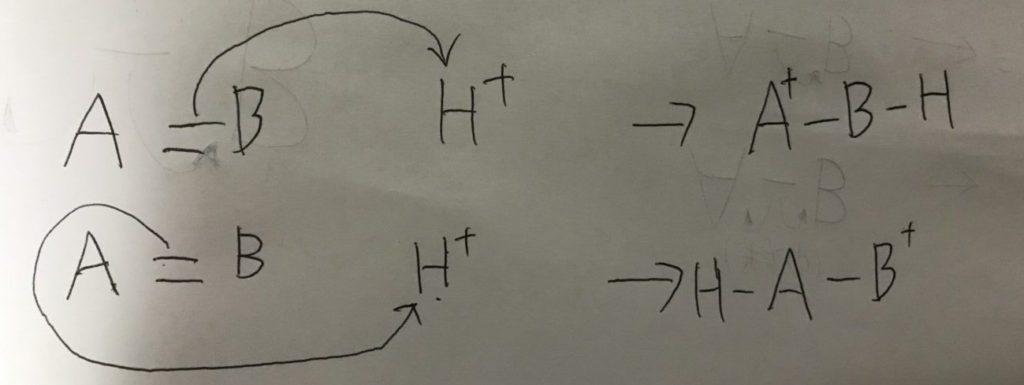
↑反応機構で電子を保持する原子。上の場合は、Bが下の場合はAが電子を共通して保持しています。
反応機構の矢印が作るもの
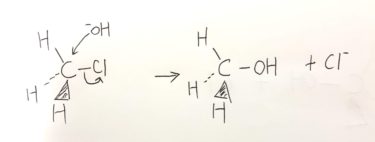
上の注意点から言えるのは、非共有電子対(ローンペア)から出た矢印は共有結合を作り、共有電子対からでた矢印は非共有電子対をつくるか別の共有結合をつくるということです。
矢印は電子の移動とともに、結合の作成も意味しうることも注意しておかなければ、思わぬ勘違いをしてしまうかもしれません。
・共有結合から矢印が出発している場合には、曲がった矢印の内側の原子が保持する。
・反応機構の矢印は、電子の移動とともに結合の作成をも意味することがある。
まとめ
いかがだったでしょうか。反応機構の矢印の意味と注意点を理解しておけば、反応機構についてより詳しくなり、さらには反応の意味をより直感的に理解することができます。
大事な要点をまとめると次のようになります。
・矢印の出発点は電子対か電子。終着点は、原子か結合
・矢印の出発点と終着点で共通して一つの原子はその電子を保持している。